嘉兴大学
- 在100℃, 101.325 kPa下有1 mol的H2O( l ),使其与100℃的大热源接触并使其向真空中蒸发,变为100℃,101.325 kPa的H2O( g ),对于这一过程可以用哪个量来判断过程的方向?( )
- 质量摩尔浓度为b的H3PO4溶液,离子平均活度因子(系数)为
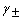 ,则电解质的活度是aB:( )。
,则电解质的活度是aB:( )。 - 浓度为b的Al2(SO4)3溶液中,正、负离子的活度因子(系数)分别为
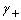 和
和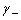 ,则离子的平均活度系数
,则离子的平均活度系数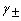 等于:( )。
等于:( )。 - 今有一球形肥皂泡,半径为r,肥皂水溶液的表面张力为σ,则肥皂泡内附加压力是:( )。
- 接触角是指:( )
- 电解质分为强电解质和弱电解质,在于:( )。
- https://image.zhihuishu.com/zhs/question-import/formula/202309/1a3a3b4de4b64527b6e37ca96c6a620b.png
- 反应A
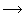 Y当实验测得反应物A的浓度[cA]与时间t成线性关系时则该反应为:( )。
Y当实验测得反应物A的浓度[cA]与时间t成线性关系时则该反应为:( )。 - pVγ = 常数(γ = Cp,m/CV,m)适用的条件是:( )
- 对恒沸混合物的描写,下列各种叙述中哪一种是不正确的?( )
- 化合物B的标准摩尔生成焓∆fH
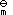 (B)的定义是:( )。
(B)的定义是:( )。 - 朗缪尔公式克描述为:( )。
- 正离子的迁移数与负离子的迁移数之和是:( )。
- https://image.zhihuishu.com/zhs/question-import/formula/202309/c630aebd95a54db1b5549e395f6a0bad.png
- 在温度T时,若电池反应1/2Cu+1/2Cl2===1/2Cu2++Cl-的标准电池电动势为E1,Cu + Cl2=== Cu2+ +2Cl- 的标准电池电动势为E2,则E1和E2的关系为:( )。
- H2和O2以2:1的摩尔比在绝热的钢瓶中反应生成H2O,在该过程中( )是正确的。
- 从同一始态出发,理想气体经可逆与不可逆两种绝热过程:( )。
- O2(g)和H2(g)的混合气体,在某一时刻,发生了如下变化:O2减少0.2 mol,H2减少0.4 mol,生成的H2O(g)是0.4 mol。若反应式为H2(g) +
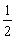 O2(g) == H2O(g) 则反应进度为:( )。
O2(g) == H2O(g) 则反应进度为:( )。 - 对行反应A
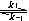 B,当温度一定时由纯A开始,下列说法中哪一点是不对的:( )。
B,当温度一定时由纯A开始,下列说法中哪一点是不对的:( )。 - 形成理想液态混合物过程的混合性质是:( )。
- 在298 K时,A和B两种气体单独在某一溶剂中溶解,遵守亨利定律,亨利常数分别为kx,A和kx,B,且知kx,A>kx,B,则当A和B压力的平衡值相同时,在一定的该溶剂中所溶解的物质的量是:( )。
- 某反应的速率系(常)数k=2.31×10-2 dm3·mol-1·s-1,当反应物初浓度1.0 mol·dm-3时反应的半衰期为:( )。
- 在串联的几个电解池中,各阳极或阴极上数值不等的物理量是:( )。
- 下列说法中( )是正确的。
- 关于液-液反应,下列说法错误的是: ( )。
- 化学吸附的吸附力是:( )。
- 零级反应AB的半衰期t1/2与A的初浓度cA,0及速率系(常)数k的关系是:( )。
- https://image.zhihuishu.com/zhs/question-import/formula/202309/e6f97fc7a9394fc4991aecf9e0e0575f.png
- B,C二组分溶液中组分B的偏摩尔吉布斯函数:
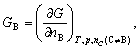 因此有:( )。
因此有:( )。 - 一定量的理想气体,从同一初态压力p1可逆膨胀到压力为p2,则等温膨胀的终态体积V(等温)与绝热膨胀的终态体积V(绝热)的关系是:( )。
- 反应PCl5(g) == PCl3(g) + Cl2(g)在473 K时的离解度为48.5%,而573 K时的离解度为97 %,则可判断为( )。
- 25℃无限稀释的KCl摩尔电导率为130 S-m2- mol-1,已知Cl-的迁移数为0.505,在K+离子的摩尔电导率为(单位:S-m2-mol-1):( )。
- 通过多相催化反应动力学的学习,可以达到以下哪些目的: ( )。
- 某坚固容器容积100 dm3,于25℃,101.3 kPa下发生剧烈化学反应,容器内压力、温度分别升至5066 kPa和1000℃。数日后,温度、压力降至初态(25℃和101.3 kPa),则下列说法中正确的为:( )。
- 通过电动势的测定,可以求难溶盐的活度积,今欲求AgCl的活度积,则应设计的原电池为:( )。
- 对于化学平衡,以下的说法中错误的是:( )。
- 对于化学反应进度,下面的表述中不正确的是:( )。
- 原电池在等温等压可逆的条件下放电时,其在过程中与环境交换的热量为:( )。
- 恒温下某电解质溶液浓度由0.1 mol-dm-3变为0.2 mol-dm-3,其摩尔电导率:( )。
- 下列各式属于偏摩尔量的是:( )。
- 由两种不互溶的纯液体A和B相互接触形成两液相时,下面说法中最符合实际情况的是: ( )
- https://image.zhihuishu.com/zhs/question-import/formula/202309/0c3d95c66645441eafdb823bcee525f7.png
- 在一定的温度和压力下,已知反应A→2B反应的标准摩尔焓变为∆rH
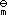 ,1(T)及反应2A→C的标准摩尔焓变为∆rH
,1(T)及反应2A→C的标准摩尔焓变为∆rH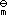 , 2(T), 则反应C→4B 的∆rH
, 2(T), 则反应C→4B 的∆rH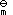 , 3(T)是:( )。
, 3(T)是:( )。 - 以C6H5C2H5为原料通过反应C6H5C2H5(g) == C6H5C2H3(g) + H2(g)制取C6H5C2H3(g)。在一定的温度和压力下该反应达平衡,若加入惰性气体而保持温度和总压力不变,则C6H5C2H5(g)的平衡转化率将( )。
- 在等温下,同组成的两个大小不同的液球的饱和蒸气压p1(大球) 和p2(小球)存在:( )。
- 反应A
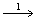 Y
Y 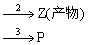 ,已知反应的活化能E2 < E3 ,为利于产物Z的生成,原则上选择:( ) 。
,已知反应的活化能E2 < E3 ,为利于产物Z的生成,原则上选择:( ) 。 - 在101 325 Pa的压力下,I2在液态水和CCl4中达到分配平衡(无固态碘存在)则该系统的条件自由度数为:( )。
- 下列说法中不正确的是( )。
- https://image.zhihuishu.com/zhs/question-import/formula/202309/99146ee682454284bf3165441dd6643a.png
- 对于实际气体玻意耳温度TB是一个重要的性质参数,当温度高于实际气体的TB时,比值pVm /RT随压力p增加的变化特征是:( )。
A:∆G B:∆S(系统)+ ∆S(环境) C:∆S(系统) D:∆S(环境)
答案:∆S(系统)+ ∆S(环境)
A:aB=4( b / b
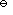 )
)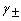 4
B:aB=27( b / b
4
B:aB=27( b / b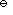 )4
)4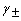 4
C:aB=27( b / b
4
C:aB=27( b / b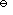 )
)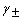 4
D:aB=4( b / b
4
D:aB=4( b / b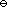 )4
)4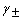 4
4答案:
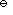
A:(
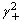 ·
·  )
)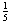 B:(
B:(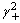 ·
· 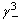 )
)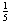 b
C:(
b
C:(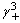 ·
· 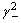 )
)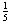 D:(108)
D:(108)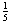 b
b答案:
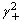
A:
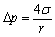 B:
B: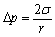 C:
C: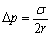
答案:
A:g/l界面经过液体至l/s界面间的夹角 B:l/g界面经过气相至g/s界面间的夹角 C:l/g界面经过气相和固相至s/l界面间的夹角 D:g/s界面经过固相至s/l界面间的夹角
答案:C:l/g界面经过气相和固相至s/l界面间的夹角
A:电解质为离子晶体和非离子晶体 B:离子间作用强和弱 C:全解离和非全解离 D:溶剂为水和非水
答案:全解离和非全解离
A:
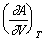 B:
B: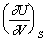 C:
C: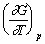 D:
D: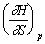
答案:
A:二级反应 B:分数级反应 C:零级反应 D:一级反应
答案:零级反应
A:理想气体绝热过程 B:理想气体绝热可逆过程 C:绝热可逆过程 D:绝热过程
答案:理想气体绝热可逆过程
A:恒沸混合物的组成随压力的改变而改变 B:其沸点随外压的改变而改变 C:平衡时,气相和液相的组成相同 D:与化合物一样,具有确定的组成
A:在温度T,由稳定态单质生成物质B时的标准摩尔焓变。书写相应的生成反应化学反应式时要使B的化学计量数νB=+1。 B:在温度T时,100 kPa压力下稳定单质生成1 mol化合物时的焓变 C:25℃和100 kPa压力下由稳定单质生成1 mol处于100 kPa下化合物的焓变 D:在100 kPa压力下各自单独存在的稳定单质化合1 mol化合物时的焓变。
A:三类吸附等温线 B:化学吸附等温线 C:五类吸附等温线 D:两类吸附等温线
A:等于1 B:小于1 C:大于1
A:不随温度变化 B:与温度的关系无法简单描述 C:随温度升高而增大 D:随温度升高而减小
A:E1/ E2= 2 B:E1/ E2= 4 C:E1/ E2= 1/2 D:E1/ E2= 1
A:∆T = 0 B:∆H = 0 C:pVγ = 常数 D:∆U = 0
A:不可能到达同一终态 B:可以到达同一终态,但给环境留下不同影响 C:可以到达同一终态
A:-0.2 mol B:-0.4 mol C:0.2 mol D:0.4 mol
A:达到平衡时正逆二向的反应速率系(常)数相等 B:反应的净速率是正逆二向反应速率之差 C:k1/ k-1的值是恒定的 D:开始时A的反应消耗速率最快
A:
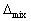 V=0 ,
V=0 ,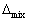 H=0 ,
H=0 , 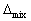 S>0 ,
S>0 , 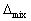 G<0
B:
G<0
B: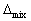 V>0 ,
V>0 ,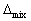 H>0 ,
H>0 , 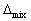 S<0 ,
S<0 , 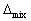 G>0
C:
G>0
C: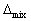 V<0 ,
V<0 ,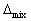 H<0 ,
H<0 , 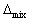 S=0 ,
S=0 , 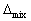 G=0
D:
G=0
D: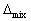 V>0 ,
V>0 ,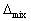 H<0,
H<0, 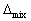 S=0 ,
S=0 , 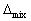 G=0
G=0
A:A的物质的量等于B的物质的量 B:A的物质的量与B的物质的量无法比较 C:A的物质的量大于B的物质的量 D:A的物质的量小于B的物质的量
A:30 s B:43.29 s C:15 s D:21.65 s
A:析出或溶解的物质的量 B:通过的电流 C:通过的电子数目 D:通过的电量
A:在等压且不作非体积功的条件下,系统吸收的热在数值上等于焓的增量 B:系统的焓等于系统在等压过程中吸收的热量 C:系统的焓等于系统所含的热量 D:只有等压过程才有焓的概念
A:整个反应是由一系列连续步骤组成的,其中每一个步骤都有一定的动力学规律 B:反应发生在不同的液相中 C:反应产物以传质方式从相界面进入两个不同的液相 D:液-液反应指的是互不相溶的液体之间的反应
A:范德华力 B:库仑力 C:化学键力
A:T1/2=2kcA,0 B:T1/2=1/(2kcA,0) C:T1/2=2k/cA,0 D:T1/2=cA,0/(2k)
A:升高温度 B:及时移走副产物P C:维持温度不变 D:降低温度
A:GB与nB有关,与T,p,nC无关 B:GB与T,p,nC,nB都有关 C:GB与nB,nC有关,与T,p无关 D:GB与T,p,nC有关,与nB无关
A:V(等温) > V(绝热) B:V(等温) < V(绝热) C:无法确定 D:V(等温) = V(绝热)
A:反应是吸热的 B:反应是放热的 C:反应的标准平衡常数K
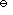 =2
D:在两温度下标准平衡常数K
=2
D:在两温度下标准平衡常数K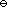 相等
相等
A:64.35 B:0.479 C:65.7 D:130
A:均是 B:鉴别在催化反应中起关键作用的表面吸附态 C:了解催化反应的详细反应机理 D:为催化反应器的设计提供依据和基础
A:该过程∆H = 0,W≠0 B:该过程∆U = 0,Q≠0 C:该过程∆U = 0,∆H = 0 D:该过程W = 0,Q≠0
A:Ag | AgCl(s) | HCl(aq) | Cl2( p
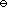 )| Pt
B:Pt | Cl2( p
)| Pt
B:Pt | Cl2( p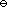 ) | HCl(aq) | AgCl(s) | Ag
C:Ag | AgCl(s)| HCl(aq) || AgNO3(aq) | Ag
D:Ag | AgNO3(aq) || HCl(aq) | AgCl(s) | Ag
) | HCl(aq) | AgCl(s) | Ag
C:Ag | AgCl(s)| HCl(aq) || AgNO3(aq) | Ag
D:Ag | AgNO3(aq) || HCl(aq) | AgCl(s) | Ag
A:化学平衡态就是化学反应的限度 B:化学平衡系统的热力学性质不随时间而变 C:化学平衡时各物质的化学势相等
A:化学反应进度与所选择表示反应进度的特殊反应物或产物无关 B:化学反应进度与化学方程式的写法无关 C:反应进度之值只能为正,单位是mol D:化学反应进度随着反应的进行而变化,其值越大,反应完成的程度越大
A:T∆S B:∆G C:∆H D:零
A:不变 B:减小 C:增大 D:不能确定
A:
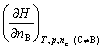 B:
B: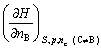 C:
C: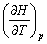
A:界面层的厚度可达几个分子层,在界面层中,A和B 两种物质的浓度处处都是均匀的 B:界面是一个界限分明的几何平面 C:界面层有几个分子层的厚度,在界面层内,A和B 两种物质的浓度沿垂直于界面方向连续递变
A:析出的固相是纯溶质 B:析出的固相一定是固溶体 C:溶质必需是挥发性的 D:析出的固相是纯溶剂
A:∆rH
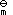 , 2(T) - 2∆rH
, 2(T) - 2∆rH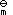 ,1(T)
B:∆rH
,1(T)
B:∆rH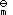 , 2(T) + ∆rH
, 2(T) + ∆rH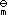 ,1(T)
C:2∆rH
,1(T)
C:2∆rH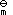 ,1(T) + ∆rH
,1(T) + ∆rH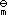 , 2(T)
D:2∆rH
, 2(T)
D:2∆rH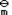 ,1(T) - ∆rH
,1(T) - ∆rH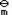 , 2(T)
, 2(T)
A:降低 B:不变 C:提高
A:p1 > p2 B:p1 = p2 C:不能确定 D:p1 < p2
A:升高温度 B:维持温度不变 C:及时移走副产物P D:降低温度
A:f’=1 B:f’=2 C:f’=0 D:f’=3
A:N种气体混合物的热力学能等于混合前N种气体的热力学能之和 B:热力学能是系统状态的单值函数 C:理想气体的热力学能只与温度有关,且与气体物质的量成正比 D:用热力学方法不能测热力学能的绝对值
A:Q = 0,W < 0,∆U > 0 B:Q = 0,W = 0,∆U = 0 C:Q < 0,W < 0,∆U < 0 D:Q < 0,W = 0,∆U < 0
A:<1 B:=1 C:>1 D:先小于1而后大于1
温馨提示支付 ¥5.00 元后可查看付费内容,请先翻页预览!
