渭南师范学院
- 化学势是一广度量。( )
- 在一个多组分溶液中,只有溶质才有偏摩尔量。( )
- 只做体积功的封闭体系,
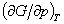 的值一定大于零。( )
的值一定大于零。( ) - 纯物质的饱和蒸气压较高的液体沸点较高。( )
- 相图中的点都是代表体系状态的点。( )
- 二元液系中若A组分对拉乌尔定律产生正偏差,那么B组分必定对拉乌尔定律产生负偏差。( )
- 凡是自由能降低的过程一定都是自发过程。( )
- 二元体系相图中,物系点移动方向是垂直上下,而相点则水平移动。( )
- 将双组分进行连续的部分气化和部分冷凝,使混合液得以分离就是精馏的原理( )
- 可逆过程中,体系对环境做功最大,而环境对体系做功最小。( )
- 定温定压且无非体积功条件下,一切吸热且熵减少的反应,均不能自发发生。( )
- 在一绝热体系中有一隔板,两边分别是空气和真空,抽去隔板,空气向真空膨胀,此时Q=0,所以ΔS=0。( )
- 带有绝热活塞(无摩擦、无质量)的一个绝热气缸装有理想气体,内壁有电炉丝,将电阻丝通电后,气体慢慢膨胀。因为是一个恒压过程Qp=ΔH,又因为是绝热体系Qp=0,所以ΔH=0。( )
- 对于真实气体混合物的反应,该反应的标准平衡常数Ky仅仅是温度的函数。( )
- 理想液态混合物与其蒸气成气、液两相平衡时,气相总压力p与液相组成xB呈线性关系。( )
- 水的相图包含一个三相点、三条实线射线、一条虚线射线和三个平面区域。( )
- 一定温度下,微溶气体在水中的溶解度与其平衡气相分压成正比。( )
- 自由能G是一状态函数,从始态I到终态II,不管经历何途径,DG总是一定的。( )
- 化学反应的平衡浓度不随时间而变化,但随起始浓度的变化而变化;化学反应的热力学平衡常数不随时间变化也不随起始浓度变化而变化。( )
- 偏摩尔量因为与浓度有关,所以它不是一个强度性质。 ( )
- 焓的定义式H = U + pV是在定压条件下推导出来的,所以只有定压过程才有焓变。( )
- 公式
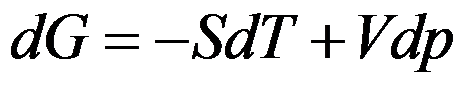 只适用于可逆过程。( )
只适用于可逆过程。( ) 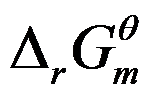 与化学反应的热力学平衡常数
与化学反应的热力学平衡常数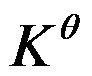 都是由反应本质决定,而与温度等外界因素无关。( )
都是由反应本质决定,而与温度等外界因素无关。( )- 完全互溶双液系T-x图中,溶液的沸点与纯组分的沸点的意义是一样的。( )
- 某理想气体从始态经定温和定容两过程达终态,这两过程的Q、W、DU及DH是相等的( )
- 在一个绝热刚瓶中,发生一个放热的分子数增加的化学反应,那么:( )
- 下面的表述中不正确的是( )
- 下述说法何者正确:( )
- 在温度为T,压力为p时,反应3O2(g)=2O3(g)的Kp与Kx的比值为:( )
- 已知苯一乙醇双液体系中,苯的沸点是353.3K, 乙醇的沸点是351.6K, 两者的共沸组成为:含乙醇47.5%(摩尔分数),沸点为341.2K。 今有含乙醇77.5%的苯溶液,在达到气、液平衡后,气相中含乙醇为y2,液相中含乙醇为 x2。下列结论何者正确?( )
- 关于节流膨胀, 下列说法正确的是( )
- 加入惰性气体对哪一个反应能增大其平衡转化率?( )
- 已知反应 3O2(g) = 2O3(g) 在25℃时rHmJ·mol-1,则对该反应有利的条件是:( )
- 有下述两种说法:(1) 自然界中,风总是从化学势高的地域吹向化学势低的地域 (2) 自然界中,水总是从化学势高的地方流向化学势低的地方。上述说法中,正确的是:( )
- 对于气相反应,当体系总压力p变化时( )
- 1mol理想气体(1)经定温自由膨胀使体积增加1倍;(2)经定温可逆膨胀使体积增加1倍;(3)经绝热自由膨胀使体积增加1倍;(4)经绝热可逆膨胀使体积增加1倍。在下列结论中何者正确?( )
- 某一固体在25℃和p 压力下升华,这意味着:( )
- 在298K、p下,两瓶含萘的苯溶液,第一瓶为2dm3 (溶有0.5mol萘),第二瓶为1dm3 (溶有0.25mol萘),若以μ1和μ2 分别表示两瓶中萘的化学势,则( )
- 在一定温度和压力下,对于一个化学反应,能用以判断其反应方向的是:( )
- 2mol A物质和3mol B物质在等温等压下混和形成液体混合物,该系统中A和B的偏摩尔体积分别为1.79 10-5m3·mol-1, 2.15 10-5m3·mol-1, 则混合物的总体积为:( )
- 理想气体从状态p1,V1,T 等温膨胀到p2,V2,T,此过程的ΔA 与ΔG 的关系为( )
- 已知373K时液体A的饱和蒸气压为133.24kPa,液体B的饱和蒸气压为66.62kPa。设A和B形成理想溶液,当溶液中A的物质的量分数为0.5时,在气相中A的物质的量分数为:( )
- 在一绝热刚壁体系内,发生一化学反应,温度从
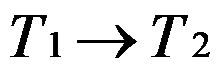 ,压力由
,压力由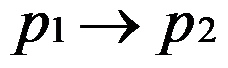 ,则( )
,则( ) - 关于焓的性质, 下列说法中正确的是( )
- 一单相体系, 如果有3种物质混合组成, 它们不发生化学反应, 则描述该系统状态的独立变量数应为( )
- 下列哪个封闭体系的内能和焓仅是温度的函数( )
- 从多孔硅胶的强烈吸水性能说明在多孔硅胶吸水过程中,自由水分子与吸附在硅胶表面的水分子比较,两者化学势的高低如何?( )
- 下列过程中, 系统内能变化不为零的是( )
- 涉及溶液性质的下列说法中正确的是( )
- 在288K时H2O(l)的饱和蒸气压为1702Pa, 0.6mol的不挥发性溶质B溶于0.540kg H2O时,蒸气压下降42Pa,溶液中H2O的活度系数γx应该为:( )
A:错 B:对
答案:错
A:错 B:对
答案:错
A:对 B:错
答案:对
A:错 B:对
答案:错
A:对 B:错
答案:错
A:错 B:对
答案:错
A:对 B:错
答案:错
A:对 B:错
答案:错
A:错 B:对
答案:对
A:错 B:对
A:错 B:对
A:错 B:对
A:错 B:对
A:错 B:对
A:错 B:对
A:错 B:对
A:错 B:对
A:对 B:错
A:对 B:错
A:错 B:对
A:错 B:对
A:错 B:对
A:对 B:错
A:对 B:错
A:错 B:对
A:Q < 0,W > 0,∆U < 0 。
B:Q = 0,W = 0,∆U < 0 ;
C:Q = 0,W = 0,∆U = 0 ;
D:Q > 0,W > 0,∆U > 0 ;
A:在定压下, 固体混合物都不会有确定的熔点
B:在定压下, 纯固体物质不一定都有确定的熔点
C:在定温下, 液体的平衡蒸气压与外压有关
D:在定压下, 纯液态物质有确定的唯一沸点
A:水的生成热即是氢气的燃烧热
B:水蒸汽的生成热即是氧气的燃烧热
C:水蒸汽的生成热即是氢气的燃烧热
D:水的生成热即是氧气的燃烧热
A:p-1
B:RT
C:(RT)-1
D:p
A:y2 = x2
B:不确定
C:y2 > x2
D:y2< x2
A:节流过程中多孔塞两边的压力不断变化
B:节流膨胀中系统的焓值改变
C:节流膨胀中系统的内能变化
D:节流膨胀是绝热可逆过程
A:3/2 H2(g) + 1/2 N2(g) = NH3(g)
B:CO(g) + H2O(g) = CO2(g) + H2(g)
C:C6H5C2H5(g) = C6H5C2H3(g) + H2(g)
D:CH3COOH(l) + C2H5OH(l) = H2O(l) + C2H5COOH3(l)
A:升温降压
B:降温降压
C:降温升压
D:升温升压
A:(1)和(2)
B:(2)
C:都不对
D:(1)
A:对Kr无影响
B:对Kf 无影响
C:对Kf 、Kr、Kp 均无影响
D:对Kp 无影响
A:S1=S4,S2=S3
B:S1= S2=S3,S4=0
C:S1=S2,S3=S4=0
D:S1= S2= S3= S4
A:三相点的压力大于p
B:三相点的压力小于p
C:固体比液体密度大些
D:固体比液体密度小些
A:μ1 = μ2
B:μ1 = 2μ2
C:μ1 = 1/2μ2
D:μ1 = 10μ2
A:Kp
B:rGm
C:rHm
D:rGm
A:9.8510-5m3
B:9.6710-5m3
C:1.00310-4m3
D:8.9510-5m3
A:ΔA>ΔG
B:ΔA=ΔG
C:无确定关系
D:ΔA<ΔG
A:1/3
B:1
C:2/3
D:1/2
A:
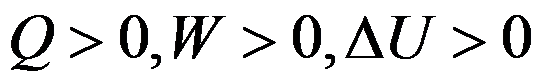
B:
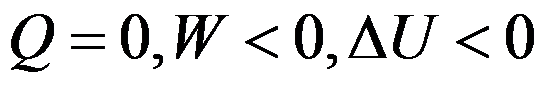
C:
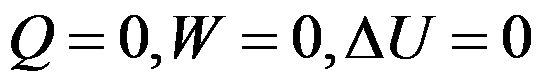
D:
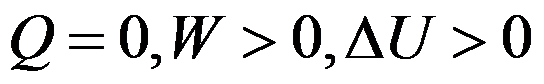
A:焓是能量, 它遵守热力学第一定律
B:焓的增量只与系统的始末态有关
C:系统的焓值等于内能加体积功
D:焓是系统内含的热能, 所以常称它为热焓
A:3个
B:6个
C:5个
D:4个
A:稀溶液
B:理想气体
C:理想溶液
D:所有气体
A:前者低
B:不可比较
C:相等
D:前者高
A:可逆循环过程
B:纯液体的真空蒸发过程
C:两种理想气体的混合过程
D:不可逆循环过程
A:理想溶液中各组分的蒸气一定是理想气体
B:溶剂服从拉乌尔定律, 其蒸气不一定是理想气体
C:溶剂中只有加入不挥发溶质其蒸气压才下降
D:溶质服从亨利定律的溶液一定是极稀溶液
A:0.9753
B:0.9948
C:0.9804
D:1.005
温馨提示支付 ¥5.00 元后可查看付费内容,请先翻页预览!







