第五章单元测试
根据酸碱质子理论,下列物质只能作碱的是
CH3NH2的共轭酸为
下面哪两种物质不属于共轭酸碱对
一元弱酸HA、HB、HC、HD的Ka依次减小,则同浓度的下列溶液pH最大的是
已知NH3的pKb = 4.75,则NH4+的酸常数pKa等于
在NH3溶液中加入固体NH4Cl,溶液的pH
在373K时,pH = 7 的溶液属于
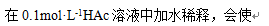
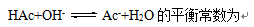
在0.1mol·L-1HCl和0.1mol·L-1HAc的混和溶液中,氢离子浓度为
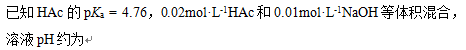

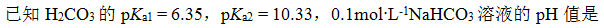
将浓度为c的氨水稀释一倍,溶液中的[OH-]为
用H3PO4(pKa1=2.16,pKa2=7.21,pKa3=12.32)和NaOH所配成的pH=7.0的缓冲溶液中,抗酸成分是
下列各组溶液中,能以一定体积比组成缓冲溶液的是
.
下列各缓冲容量最大的是溶液
NaHCO3为两性物质,其酸常数Ka和碱常数Kb的乘积等于Kw。
水中加入强酸,由水解离出的氢离子和氢氧根离子浓度都减少,因此水的离子积减少。
缓冲溶液的缓冲范围与共轭酸的解离常数有关,与溶液pH关系不大。
A: NH4+ B: H2O C: HCO3- D: Ac-
答案: Ac-
A: CH3NH3+ B: CH3NH- C: CH2NH3+ D: CH4+NH2
A: HAc-Ac- B:H2PO4--HPO42- C: NH4+-NH3 D: CO32--H2CO3
A: NaB B: NaC C: NaD D: NaA
A: 5.25 B: 9.25 C: 4.75 D: 7.00
A:不变 B:可能变小,也可能变大 C: 变大 D: 变小
A: 碱性 B: 酸性 C: 不能确定 D: 中性
A: Ka(HAc)减少,pH增大 B: Ka(HAc)增大,pH增大 C: Ka(HAc)不变,pH减小 D: Ka(HAc)不变,pH增加
A:
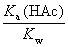 B:
B: 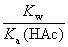 C: Ka(HAc)
D: KwKa(HAc)
C: Ka(HAc)
D: KwKa(HAc)
A:0.1mol·L-1<[H3O+]<0.2mol·L-1 B:[H3O+] = 0.1mol·L-1 C:[H3O+]>0.2mol·L-1 D:[H3O+] = 0.2mol·L-1
A: 4.76 B: 3.38 C: 2 D: 9.24
A: NaHCO3 B: Na2HPO4 C: Na2CO3 D: Na3PO4
A: 6.35 B: 7.00 C: 8.34 D: 10.33
A:
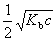 B:
B: 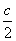 C:
C: 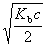 D: 2c
D: 2c
A: H2PO4- B: H3O+ C: H3PO4 D: HPO42-
A: 浓度均为0.1mol·L-1的NaAc溶液和HAc溶液 B: 浓度均为0.1mol·L-1的HAc溶液和HCl溶液 C: 浓度均为0.1mol·L-1的NaOH溶液和HCl溶液 D: 浓度均为0.1mol·L-1的NaOH溶液和NH3溶液
A: 500mL中含有0.1molHAc和0.1molNaAc B: 500mL中含有0.05molHAc和0.15molNaAc C: 500mL中含有0.15molHAc和0.05molNaAc D: 1000mL中含有0.15molHAc和0.05molNaAc
A:错 B:对
A:错 B:对
A:对 B:错
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!
