第九章单元测试
在下列化合物中C原子采用sp杂化的是
中心原子采用不等性sp3杂化的分子是
中心原子采用sp2杂化的分子是
几何构型为直线形的是
分子之间同时存在色散力、诱导力、取向力的是
分子之间色散力最大的是
分子之间只存在色散力的是
能形成分子内氢键的分子是
原子形成共价键的数目等于基态原子的未成对电子数。
σ键是原子轨道沿键轴方向以“头碰头”方式重叠形成的,原子轨道的重叠部分沿键轴呈圆柱形对称分布。
s电子与s电子配对形成的键一定是σ键,p电子与p电子配对形成的键一定为π键。
非极性分子中的化学键不一定是非极性键。
NH3和H2O分子中的中心原子均发生sp3杂化,但氧原子的2对孤对电子占据2个杂化轨道而产生更大的斥力,使O-H键键角小于氨分之中N-H键键角。
π键电子云重叠程度较σ键大,所以π键比σ键稳定。
C-C单键的键能是C≡C叁键键能的三分之一。
键能是同种键各级解离能的平均值。
键能与键长有关,通常是键越长,键能越大。
配位键是通过成键原子中的一个单独提供电子对共用而形成的,所以配位键不属于共价键。
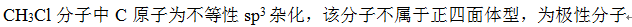 。
。
A:CH3Cl
B:C2H4
C:C2H2
D:CH4
答案:C2H2
A:CCl4 B:BCl3 C:AlCl3 D:PCl3
A:SiF4
B:NH3
C:BCl3
D:H2S
A:BF3
B:CO2
C:CH4
D:H2S
A:Br2
B:CS2
C:NH3
D:CCl4
A:H2 B:Br2 C:I2 D:Cl2
A:CCl4 B:HF C:NH3 D:CH3CH2OH
A:CH3CH2OH B:HNO3 C:对硝基苯酚 D:CHCl3
A:对 B:错
A:对 B:错
A:对 B:错
A:错 B:对
A:对 B:错
A:错 B:对
A:对 B:错
A:对 B:错
A:对 B:错
A:错 B:对
A:错 B:对
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!
