第七章测试1.原子吸收光谱是由下列哪种跃迁产生的( )
A:激发态原子的内层电子 B:基态原子的内层电子 C:基态原子的外层电子 D:激发态原子的外层电子
答案:C
2.原子发射光谱中,常用的光源有( )
A:电弧、电火花、电感耦合等离子炬等 B:钨灯、氢灯和氘灯 C:空心阴极灯 D:棱镜和光栅 3.在原子吸收法中,火焰的作用是使基态原子变成激发态原子或离子。( )
A:对 B:错 4.用原子发射光谱分析法分析污水中的Cr、Mn、Cu、Fe等(含量为10-6数量级),应选用下列哪种激发光源( )
A:直流电弧 B:电感耦合等离子炬 C:高压火花 D:火焰 5.在原子发射光谱的光源中,激发温度最高的光源为 ( )
A:电火花 B:直流电弧 C:交流电弧 D:ICP 6.原子化器的主要作用是( )
A:将试样中的待测元素转化为气态的基态原子 B:将试样中的待测元素转化为中性分子 C:将试样中的待测元素转化为离子 D:将试样中的待测元素转化为激发态原子 7.空心阴极灯中对发射线宽度影响最大的是( )
A:阳极材料 B:阴极材料 C:灯电流 D:填充气体 8.原子吸收光谱法是一种成分分析方法, 可对六十多种金属和某些非金属元素进行定量测定, 它广泛用于( )的定量测定。
A:元素定性 B:低含量元素 C:高含量元素 D:极微量元素 9.原子吸收光谱法常用的光源是: ( )
A:空心阴极灯 B:氢灯; C:电弧; D:火焰; 10.在原子吸收分析中,过大的灯电流除了产生光谱干扰外,还使发射共振线的谱线轮廓变宽,这种变宽属于自然变宽。( )
A:对 B:错 1.难溶电解质
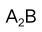 的饱和溶液中,
的饱和溶液中,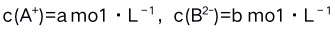 ,则其
,则其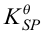 为( )。
为( )。A:
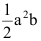 B:
B: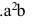 C:
C: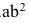 2.某溶液中含有
2.某溶液中含有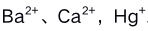 三种离子浓度均为0.01 ,向溶液中滴加
三种离子浓度均为0.01 ,向溶液中滴加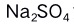 溶液,则各离子开始沉淀形成的沉淀顺序为( )。已知
溶液,则各离子开始沉淀形成的沉淀顺序为( )。已知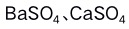 、
、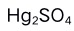 的
的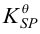 分别为
分别为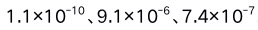 。
。A:
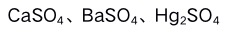 B:
B: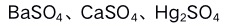 C:
C: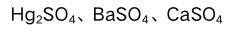 D:
D: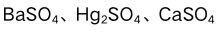 3.在
3.在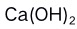 沉淀的饱和溶液中加入
沉淀的饱和溶液中加入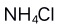 固体后,
固体后,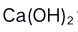 沉淀的量( )
沉淀的量( )A:增多 B:减少 C:无法判断 D:不变 4.沉淀滴定法中,指示剂用量必须合适,下列说法不正确的是( )
A:指示剂有颜色,可能会影响终点颜色判断 B:指示剂也是弱酸弱碱,会影响滴定终点 C:指示剂本身的颜色没有干扰 D:指示剂用量过少,会使滴定延后 5.莫尔法沉淀滴定法中使用的指示剂是( )
A:
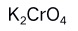 B:铁铵矾
C:NaCl
D:荧光黄
6.可以利用分步沉淀原理对溶液中几种离子进行分离,若难溶电解质的溶度积常数相差越大,分离就越完全。( )
B:铁铵矾
C:NaCl
D:荧光黄
6.可以利用分步沉淀原理对溶液中几种离子进行分离,若难溶电解质的溶度积常数相差越大,分离就越完全。( )A:错 B:对 7.将
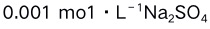 溶液与
溶液与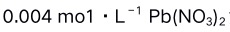 溶液等体积混合,能产生
溶液等体积混合,能产生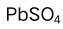 沉淀。已知
沉淀。已知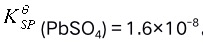 。( )
。( )A:对 B:错 8.AgCl可溶于氨水,是由于生成了配位化合物。( )
A:对 B:错 9.难溶电解质溶液中离子浓度的乘积就是该物质的溶度积。( )
A:对 B:错 10.佛尔哈德法是以铁铵矾为指示剂,分直接滴定法和返滴定法。( )
A:错 B:对 1.莫尔法可用于测定 等能与 生成沉淀的离子。( )
A:对 B:错 2.溶度积常数大的沉淀的溶解度不一定也大。
A:错 B:对 3.盐效应和酸效应都会使沉淀的溶解度增大。
A:错 B:对 4.在重量分析中,一般加过量的沉淀剂,利用同离子效应降低沉淀的溶解度,但沉淀剂过量不能太多,否则会由于盐效应或配位效应增大沉淀的溶解度。
A:对 B:错 5.氟化钙的溶解度在pH=5的溶液中较在pH=3的溶液中为大
A:对 B:错 6.
测定含铝试样中Al的含量,试样经溶解后,消除干扰,加氨水使之生成氢氧化铝沉淀,经过滤、洗涤后灼烧成氧化铝后称量,计算Al含量的换算因数为( )。
A:
![]()
![]()
![]()
![]()
A:在稀溶液中加热,加电解质,溶液后立即过滤 B:在稀溶液中加热慢慢加入沉淀剂且不断搅拌,要陈化 C:在浓溶液中加热,加电解质,沉淀后陈化 D:在浓溶液中加热,慢慢加入溶液剂,沉淀后立即过滤 8.在难溶电解质的饱和溶液中,加入其它易溶强电解质会使难溶电解质的溶解度比同温度时在纯水中的溶解度增大。这种现象称为( )。
A:酸效应 B:同离子效应 C:盐效应 D:配位效应 9.下列不属于重量分析对称量形式要求的是( )。
A:有较大的摩尔质量 B:与沉淀形式相同 C:对空气有足够的化学稳定性 D:组成已知,且固定 10.沉淀形成后,需要进行陈化的是
A:二者都需要 B:无定形沉淀 C:二者都不需要 D:晶型沉淀 1.弱酸溶液越稀,其解离度越大,所以溶液中的H+浓度越大。( )
A:对 B:错 2.根据质子理论,凡是给出质子的物质是碱,凡是接受质子的是酸。( )
A:错 B:对 3.把pH=3和pH=5的两稀酸溶液等体积混合后,混合液的pH值应等于4。 ( )
A:错 B:对 4.可以利用同离子效应来控制某些酸根离子的浓度,从而达到分离某些混合离子的目的。( )
A:对 B:错 5.按照酸碱质子理论,下列物质中即可作为酸又可以作为碱的是( )。
A:S2-
B:〔Al(H2O)6〕3+
C:HCO3-
D:PO43-
6.计算NH4Ac的溶液中H+浓度的最简式为( )
A:
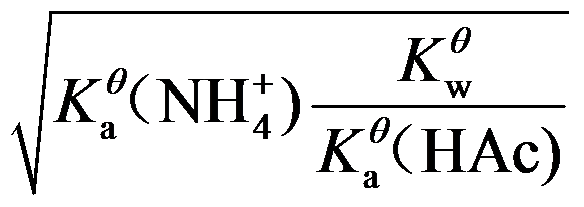
B:
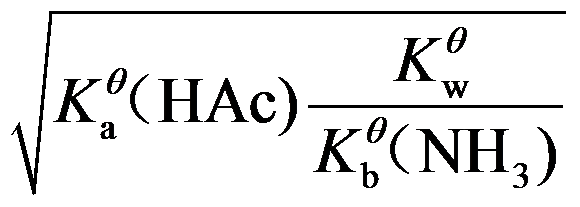
C:
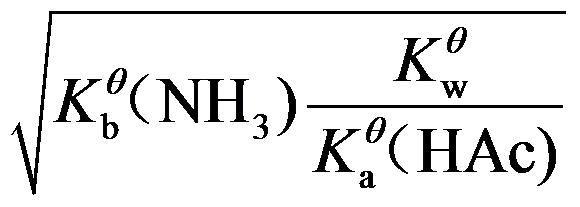
D:
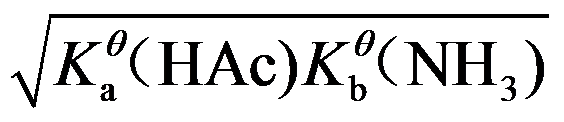
7.已知:Kaθ(HAc)=1.75×10-5, Kaθ(HCN)=6.2×10-10, Kaθ(HF)=6.6×10-4, Kbθ(NH3·H2O)=1.8×10-5。下列溶液的浓度均为0.1 mol·L-1,其溶液pH按由大到小的顺序排列正确的是( )
A:NaCN>NaAc>NaF>NaCl>NH4Cl
B:NaAc>NaCN>NaF>NaCl>NH4Cl
C:NaF>NaAc>NaCN>NaCl>NH4Cl
D:NH4Cl>NaCl>NaF>NaAc>NaCN
8.已知Ka1Ө(H2S) =1.1×10-7 ,Ka2Ө (H2S) = 1.3 ×10-13,在0.10 mol·L-1的HCl溶液中通入H2S至饱和,则溶液中S2-的浓度为( )
A:1.4×10-17
B:1.4×10-19
C:1.4×10-20
D:1.4×10-18
9.在酸碱滴定中,选择指示剂可不必考虑的因素是( )
A:指示剂的变色范围
B:指示剂的分子结构
C:指示剂的颜色变化
D:pH突跃范围
10.下列能做缓冲溶液的是:( )
A:60ml 0.1mol·L-1 HAc和30ml 0.1mol·L-1 NaOH混合液
B:0mL 0.1mol·L-1 HAc和30mL 0.1mol·L-1 HCl混合液
C:60mL 0.1mol·L-1 NaCl和30mL 0.1mol·L-1 NH4Cl混合液
D:60ml 0.1mol·L-1 HAc和30mL 0.2mol·L-1 NaOH混合液
11.将50.0mL0.100mol.L-1(NH4)2SO4溶液,加入到50.0mL 0.200mol.L-1 NH3·H2O溶液中,得到的缓冲溶液pH值是(Kbө(NH3·H2O)=1.8×10-5)( )
A:8.70
B:9.56
C:9.26
D:9.00
12.已知HAc的pKa=4.74,则在pH=4时,HAc和Ac-的分布分数分别为( )
A:0.25 和0.75
B:0.85 和0.15
C:0.75 和0.25
D:0.15 和0.85
1.
下列配合物命名不正确的是
A:
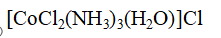 氯化二氯·三氨·一水合钴(III)
氯化二氯·三氨·一水合钴(III)
 六氯合铂(IV)酸
六氯合铂(IV)酸
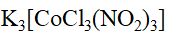 三硝基·三氯合钴(III)酸钾
三硝基·三氯合钴(III)酸钾
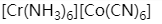 六氰合钴(III)酸六氨合铬(III)
六氰合钴(III)酸六氨合铬(III)
下列配合物中,在水溶液中解离度最小的是
A:
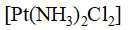
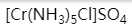
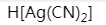
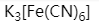
在配离子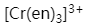 中,形成体是
中,形成体是 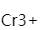 ,配位数为6。
,配位数为6。
A:错 B:对 4.
配合物 中配离子的电荷数为 +2,中心原子为Fe,中心离子的配位数为6 。
中配离子的电荷数为 +2,中心原子为Fe,中心离子的配位数为6 。
A:对 B:错 5.
与一个形成体成键的配体的数目,称为该形成体的配位数。
A:对 B:错 6.
EDTA在水溶液中有七种存在形式,各种存在形式的浓度相对大小取决于溶液的pH值。
A:错 B:对
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!