第四章单元测试
- 某反应,当温度从
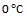 升高到
升高到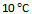 ,反应速率变为原来的4倍,若从
,反应速率变为原来的4倍,若从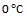 升高到
升高到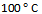 , 则反应速率变为原来的40倍。( )
, 则反应速率变为原来的40倍。( ) - 一反应
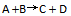
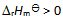 升高温度使平衡向右移动是因为温度升高时,正反应速率
升高温度使平衡向右移动是因为温度升高时,正反应速率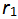 升高,逆反应速率
升高,逆反应速率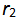 降低造成的。( )
降低造成的。( ) - 反应系统中加入催化剂后,虽然降低了Ea,但
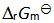 不会因此改变。( )
不会因此改变。( ) - 下列哪种情况系统到达平衡所需时间最少 ( )
- 若反应
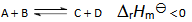 当反应的体系的温度升高时,将会有( )
当反应的体系的温度升高时,将会有( ) - 6、下列说法正确的是( )
- 7、下列说法正确的是( )
- 8、下列说法正确的是( )
- 9、某分解反应,当反应物浓度为 0.2
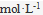 时,反应速度为 0.3
时,反应速度为 0.3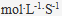 ,如果这个反应为二级反应,当反应物浓度为 0.6
,如果这个反应为二级反应,当反应物浓度为 0.6 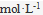 时,这个反应的反应速度 (
时,这个反应的反应速度 (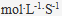 ) 将是( )
) 将是( ) - 10、反应速度随着温度升高而加快的主要理由是( )
- 11、反应
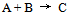 为一基元反应,该反应的速度常数的单位应当是( )
为一基元反应,该反应的速度常数的单位应当是( ) - 12、反应
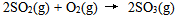 的反应速率可以表示为
的反应速率可以表示为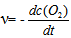 ,也可以表示为( )
,也可以表示为( ) - 13、有一化学反应
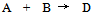 , 三次实验数据如下:
, 三次实验数据如下:
初始(A)∕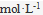 初始(B)∕
初始(B)∕ 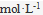 生成D的初始速率(
生成D的初始速率(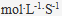 )
)
0.03 0.03 0.3 × 10 -4
0.06 0.06 1.2 × 10 -4
0.06 0.09 2.7 × 10 -4
该反应的速率方程式为( ) - 14、正反应的活化能
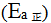 大于逆反应的活化能
大于逆反应的活化能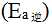 ,则正反应的标准 摩尔焓变( )
,则正反应的标准 摩尔焓变( ) - 15、不会影响反应速率常数k的因素( )
- 16、如图所示,反应
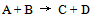 所涉及的焓相对大小为:
所涉及的焓相对大小为: 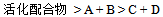 ,因此:( )
,因此:( ) - 已知反应
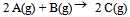 的
的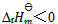 。下列哪一项叙述是正确的( )
。下列哪一项叙述是正确的( ) - 对某一化学反应,随着反应的进行将发生下列哪项变化( )
- 300K时鲜牛奶4小时变质,但在277K 时保存48小时,则牛奶的活化能为( )
- 503K时的反应的活化能为184.1 KJ·mol-1,若加入催化剂后变为104.6 KJ·mol-1,此时正反应速率增加的倍数为( )
- 下列表述中正确的是( )
- 下列叙述中正确的是( )
A:错 B:对
答案:错
A:错 B:对
A:错 B:对
A:
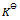 接近于1
接近于1B:
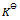 很大
很大C:
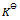 很小
很小D:无法判断
A:
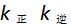 都增大,同时Ky 减小
都增大,同时Ky 减小B:
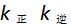 都减小,同时Ky 增大
都减小,同时Ky 增大C:
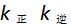 减小,同时Ky 增大
减小,同时Ky 增大D:
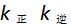 增大,同时Ky减小
增大,同时Ky减小A:零级反应的速度常数k的单位为
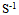
B:当所有反应物的浓度加倍时,反应速度也加倍,那么这个反应必定是一级反应
C:反应
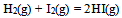 的速率方程为
的速率方程为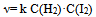 , 则该反应为基元反应
, 则该反应为基元反应D:
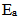 较大的反应,k必定大
较大的反应,k必定大A:对于一个正向为吸热的反应来说,如果升高温度,正向反应速度必然增加,逆向反应速度减少
B:同一化学反应,当条件变更时,活化能减少,反应速度也随之减少
C:正逆反应的活化能数值相等、符号相反
D:活化分子的平均能量与反应物分子平均能量的差值称为活化能
A:提高温度,对活化能较大的反应,反应速率的增加比活化能小的要大
B:有反应Ⅰ、Ⅱ, 298K时反应速率
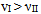 ,而318K时
,而318K时 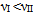 ,则
,则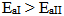
C:零级反应的速率与反应物的浓度有关
D:质量作用定律适用于基元反应也适用于复杂反应
A:2.70
B:0.30
C:0.90
D:0.60
A:高温下分子的能量增加,使每次碰撞能量增大
B:活化分子随温度升高而减少
C:高温下分子碰撞次数增多
D:活化分子百分数随温度升高而增加
A:
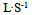
B:
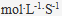
C:
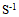
D:
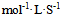
A:
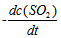
B:
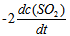
C:
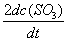
D:
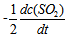
A:
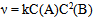
B:
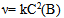
C:
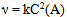
D:
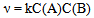
A:
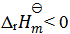
B:
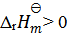
C:
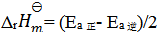
D:无法确定
A:反应温度
B:催化剂
C:反应活化能
D:改变反应物浓度
A:该反应是不可逆的.
B:逆反应的活化能低于正反应活化能.
C:该反应不可能有催化剂.
D:该反应是放热的.
A:由于
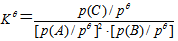 ,随着反应的进行,
,随着反应的进行,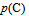 逐渐增大,
逐渐增大,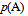 ,
, 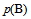 逐渐减小,平衡常数逐渐增大。
逐渐减小,平衡常数逐渐增大。B:升高温度,
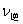 增大,
增大,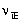 减小,将导致平衡向左移动
减小,将导致平衡向左移动 C:增加压力,使
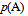 、
、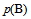 增大,
增大,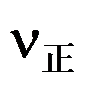 增大,平衡向左移动
增大,平衡向左移动 D:加入催化剂,同等程度的加快正、逆反应的速率,加速达到平衡
A:活化能减小
B:速率常数变小
C:平衡常数变小
D:反应速率降低
A:
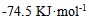
B:无法计算
C:
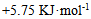
D:
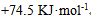
A:
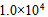
B:
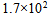
C:
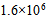
D:
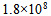
A:k不随温度变化
B:
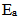 较大的反应,k必定大
较大的反应,k必定大C:V正通常随时间而减小
D:k值与催化剂的加入无关
A:凡速率方程式中各物质浓度的指数等于反应方程式中各反应物的计量系数,此反应为基元反应
B:非基元反应是由若干个基元反应组成的
C:反应速率与反应物浓度的乘积成正比
D:反应级数等于化学反应式中各反应物计量系数和
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!