第九章单元测试
- 下列分子中键角最大的是( )
- 下列说法中正确的是 ( )
- 下列分子间只存在色散力、诱导力和取向力的是( )
- 在下列化合物中,不具有孤电子对的是( )
- 下列说法正确的是( )
- 下列说法正确的是:( )
- 下列说法正确的是:( )
- 下列说法正确的是:( )
- 下列分子间既存在诱导力,又存在取向力的是:( )
- 形成HCl 分子时原子轨道重叠是( )
- SiCl4、C2H4 分子中( )
- 下列分子中既具有极性键又有非极性键的是( )
- 中心原子仅以SP杂化轨道成键的是( )
- 用价层电子对互斥理论判断
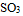 的分子构型是( )
的分子构型是( ) 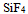 、
、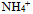 和
和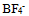 具有相同空间构型,其构型是( )
具有相同空间构型,其构型是( )- 下列物质中,只需克服色散力就能沸腾的是( )
- 下列说法中正确的是( )
- 下列说法中正确的是( )
- 下列说法中错误的是( )
- 下列哪些叙述是正确的( )
- 下列哪个分子的偶极矩不等于零( )
- 下列分子中,其中心原子采用sp杂化轨道的是( )
- 下列
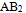 型分子中,具有直线形结构的是( )
型分子中,具有直线形结构的是( ) - 下列分子或离子的中心原子都是等性
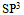 杂化,且空间构型是四面体形的是( )
杂化,且空间构型是四面体形的是( ) - 下列分子间只存在色散力和诱导力的是( )
A:
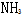
B:
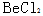
C:
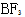
D:
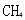
答案:
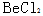
A:
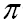 键较活泼,易发生反应
键较活泼,易发生反应 B:双键键能是单键键能的两倍
C:阴离子总比阳离子大
D:任何分子中
 键的键长均相等
键的键长均相等A:
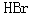 气体
气体 B:
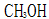 和
和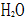
C:
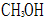 和
和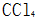
D:
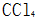 和
和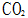
A:
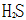
B:

C:
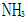
D:
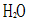
A:
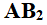 型共价化合物中,其中心原子均采用SP杂化轨道成键。
型共价化合物中,其中心原子均采用SP杂化轨道成键。B:凡是中心原子采用
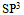 杂化轨道成键的分子,其几何构型为正面四体。
杂化轨道成键的分子,其几何构型为正面四体。C:
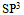 杂化可分为等性
杂化可分为等性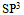 杂化与不等性
杂化与不等性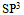 杂化。
杂化。D:
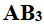 型共价化合物,其中心原子均采用
型共价化合物,其中心原子均采用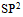 杂化轨道成键。
杂化轨道成键。A:C=C的键能的一半大于C—C的键能,小于2倍的C—C的键能
B:两原子以共价单键结合时,化学键为
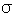 键;以共价多重键结合时,化学键均为π键
键;以共价多重键结合时,化学键均为π键C:对于多原子分子来说,只要分子结构对称,该分子一定是非极性分子
D:杂化轨道参与而形成的化学键一般都是
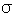 键
键A:色散力仅存在非极性分子之间
B:
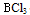 分子的空间构型是平面三角形,而
分子的空间构型是平面三角形,而 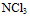 分子的空间构型是三角锥形
分子的空间构型是三角锥形C:所谓SP3杂化,是指1个S电子与3个P电子混杂
D:一种元素的原子最多所能形成共价单键的数目,等于基态的该种元素原子中所含未成对电子数
A:由电负性相同的元素的原子组成的分子,也必定是非极性分子
B:杂化轨道的数目与参与杂化的轨道数目一定相等
C:共价键皆有饱和性和方向性
D:成键原子的价电子层中若无未成对电子,就不能形成共价键
A:
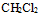 和
和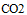
B:
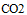 气体
气体C:
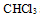 和
和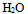
D:
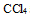 和苯
和苯A:
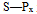 重叠
重叠B:
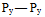 重叠
重叠C:S—S 重叠
D:
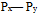 重叠
重叠A:分子中都有π键
B:不都属于非极性分子
C:属于极性分子
D:分子中都有杂化轨道成键
A:
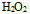
B:
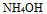
C:
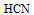
D:
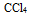
A:
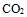 和
和 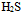
B:
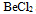 和
和 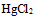
C:
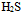 和
和 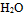
D:
 和
和 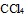
A:正四面体
B:V型
C:平面三角形
D:三角锥形
A:三角锥形
B:正方形
C:四边形
D:正四面体
A:
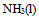
B:
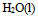
C:
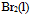
D:
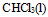
A:Be的外层电子是
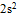 ,激发到一个
,激发到一个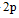 轨道上,就能形成
轨道上,就能形成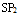 杂化轨道
杂化轨道B:在HC≡CH分子中,有两个π键,在
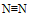 中,也有两个π键,故
中,也有两个π键,故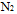 分子也很活泼
分子也很活泼C:由同种元素组成的双原子分子,必定是非极性分子
D:硼原子只有一个未成对的电子,故只能形成一价的化合物
A:非极性分子的偶极矩等于零
B:双键,有一个
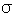 键和一个π键,所以它比单键的化学性稳定
键和一个π键,所以它比单键的化学性稳定C:
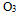 是非极性分子
是非极性分子D:碳和氧的电负性差值大于氢和氯的电负性差值,故CO的极性比HCl的大
A:
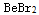 和
和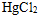 都具有sp杂化轨道形成的键
都具有sp杂化轨道形成的键B:具有四面体构型的分子,其中心原子采用的杂化轨道是
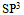 ,凡是中心原子采用
,凡是中心原子采用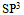 杂化轨道的分子,其空间构型必定是四面体
杂化轨道的分子,其空间构型必定是四面体C:键合原子之间如果存在叁键,则其成键轨道多是sp杂化轨道,反之以sp杂化轨道成键的分子不一定具有叁键
D:
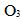
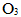 分子中,有
分子中,有 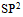 杂化轨道形成的键
杂化轨道形成的键A:多原子分子中,键的极性越强,分子极性越强
B:分子中的键为非极性键,分子不一定是非极性分子
C:非极性分子中的化学键,一定是非极性的共价键
D:具有极性共价键的分子,一定是极性分子
A:
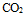
B:
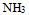
C:
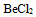
D:
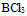
A:
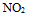
B:

C:
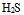
D:
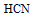
A:
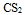
B:
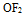
C:
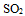
D:
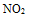
A:
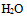
B:
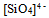
C:
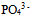
D:
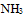
A:
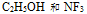
B:
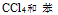
C:
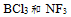
D:
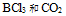
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!