第五章单元测试
- 1、弱酸浓度越小,
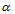 值越大,故pH越低。( )
值越大,故pH越低。( ) - 2、在HAc溶液中,加入NaAc越多,HAc离解得越少。( )
- 3、下列能做缓冲溶液的是 ( )
- 4、在氨水中加入少许
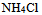 后,
后,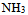 将 ( )
将 ( ) - 5、一元弱酸HA的
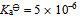 ,则
,则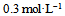 溶液的pH值等于( )
溶液的pH值等于( ) - 6、将物质的量浓度相等的NaOH和HAc溶液等体积混合后,混合液中有关离子的物质的量浓度间确定存在的关系是( )
- 7、在25℃时,
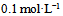 某一元弱酸溶液的电离度为0.2%,则此溶液的
某一元弱酸溶液的电离度为0.2%,则此溶液的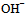 浓度为( )
浓度为( )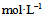
- 下列说法不正确的是( )
- 将
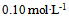 的HAc溶液加水稀释至原体积的2倍时,其
的HAc溶液加水稀释至原体积的2倍时,其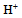 浓度和PH的变化趋势各为( )
浓度和PH的变化趋势各为( ) - 下列叙述中不正确的是( )
- 将1升4
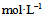 氨水与1升2
氨水与1升2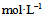 盐酸溶液混合,混合后OH-离子浓度为( )
盐酸溶液混合,混合后OH-离子浓度为( )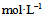
- 根据平衡移动原理,在0.10
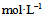 HAc溶液种,下列说法不正确的是( )
HAc溶液种,下列说法不正确的是( ) - 下列溶液中缓冲能力最大的是( )
- 0.025
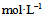 HAc溶液与等体积NaAc溶液相混,要使pH维持4.05,混合后酸和盐的浓度比应为( )
HAc溶液与等体积NaAc溶液相混,要使pH维持4.05,混合后酸和盐的浓度比应为( ) - 用
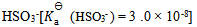 和
和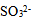 配制的缓冲溶液的pH范围( )
配制的缓冲溶液的pH范围( ) - 对于下列反应
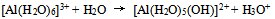 正确的叙述是( )
正确的叙述是( ) 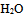 、
、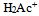 、
、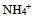 的共轭碱性强弱顺序是( )
的共轭碱性强弱顺序是( )- 反应
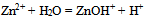 的
的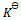 值为
值为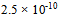 ,则
,则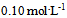 的该溶液的pH值是( )
的该溶液的pH值是( ) - 均为
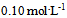 的三种盐溶液:
的三种盐溶液: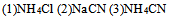 这三种盐溶液pH从大到小的顺序是( )
这三种盐溶液pH从大到小的顺序是( ) - 向
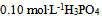 溶液中滴加
溶液中滴加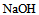 溶液至pH=8.0,溶液中浓度最大的磷酸型体是( )。已知:
溶液至pH=8.0,溶液中浓度最大的磷酸型体是( )。已知: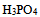 的
的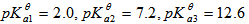
- 在110ml浓度为
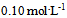 的HAc中,加入10ml浓度为
的HAc中,加入10ml浓度为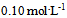 的NaOH溶液,则混合溶液的pH值为( )(已知HAc的
的NaOH溶液,则混合溶液的pH值为( )(已知HAc的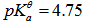 )
) - 在
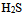 的饱和水溶液中,下列浓度关系正确的是( )
的饱和水溶液中,下列浓度关系正确的是( ) 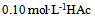 溶液在1升
溶液在1升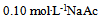 水溶液中,HAc的电
水溶液中,HAc的电
离度为( )- 0.20
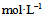 甲酸溶液中3.2%的甲酸已电离,它的电离常数是( )
甲酸溶液中3.2%的甲酸已电离,它的电离常数是( ) - 如果乙酸的离解常数是1.75 × 10-5
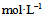 ,则以什么比例混合乙酸和乙酸钠得到pH=6.2的缓冲溶液( )
,则以什么比例混合乙酸和乙酸钠得到pH=6.2的缓冲溶液( ) 根据下列质子传递反应, 最强的质子碱是()
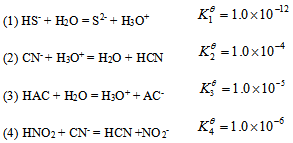
A:对 B:错
答案:错
A:错 B:对
A:
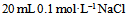 和
和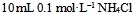 混合液
混合液B:
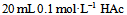 和
和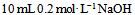 混合液
混合液C:
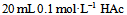 和
和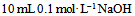 混合液
混合液D:
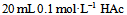 和
和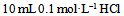 混合液
混合液A:
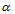 、pH 都减小
、pH 都减小B:
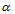 减小,pH 增大
减小,pH 增大C:
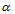 增大,pH 变小
增大,pH 变小D:
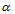 、pH 都增大
、pH 都增大A:5.30
B:2.91
C:2.39
D:5.82
A:
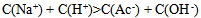
B:
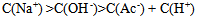
C:
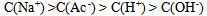
D:
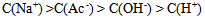
A:
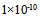
B:
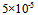
C:
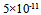
D:
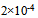
A:用HCl溶液中和pH相同,体积相等的
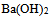 和NaOH溶液,所需HCl的量相等
和NaOH溶液,所需HCl的量相等B:用NaOH中和物质的量浓度相同,体积相等的HAc和HCl溶液,所需NaOH的量相等
C:用NaOH中和pH相同,体积相等的HAc和HCl溶液,所需NaOH的量相等
D:用HCl中和物质的量浓度和体积相同的KOH和
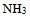 水溶液所需HCl的量相等
水溶液所需HCl的量相等A:减小和增加
B:增加和减小
C:为原来的一倍和减小
D:为原来的一半和增大
A:对于弱酸溶液,浓度越小,电离度越大,氢离子浓度越大;
B:对于弱碱溶液,当加水稀释时,pH值减小
C:对于弱电解质溶液,同离子效应使其电离度减小,盐效应使其电离度增加
D:在多元弱酸的稀溶液中,二元酸根的浓度近似等于其最后一级的离解平衡常数
A:1
B:2
C:
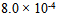
D:
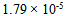
A:用水稀释,离解度增大
B:加入少量HCl溶液,HAc的离解度减少
C:加入少NaOH溶液,平衡向右移动
D:加入浓HAc,由于增加反应物浓度,平衡向右移动,结果HAc离解度增大
A:
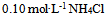 水0.1升
水0.1升B:
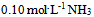 水0.5升与
水0.5升与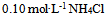 水0.05升的混合液
水0.05升的混合液C:
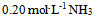 水0.5升与
水0.5升与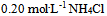 水0.05升的混合液
水0.05升的混合液D:
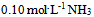 水0.1升
水0.1升A:5 : 1
B:6 : 1
C:30 : 1
D:50 : 1
A:2.4~4.0
B:6.5~8.5
C:10~12
D:2~4
A:
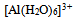 是酸,而
是酸,而 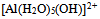 是它的共轭碱
是它的共轭碱B:
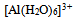 是酸,而
是酸,而 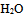 是它的共轭碱
是它的共轭碱C:
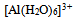 是碱,而
是碱,而 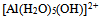 是它的共轭酸
是它的共轭酸D:
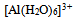 是碱,而
是碱,而 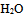 是它的共轭酸
是它的共轭酸A:
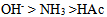
B:
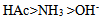
C:
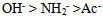
D:
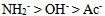
A:4.34
B:5.30
C:6.78
D:3.25
A:(2) > (1) > (3)
B:(1) > (3) > (2)
C:(2) > (3) > (1)
D:(1) > (2) > (3)
A:
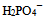
B:
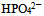
C:
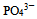
D:
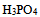
A:2.75
B:3.75
C:4.75
D:5.75
A:
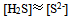
B:
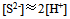
C:
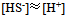
D:
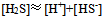
A:100
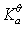 /0.1%
/0.1%B:100
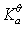 %
% C:1000
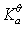 %
% D:10
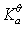 %
% A:
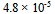
B:
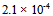
C:
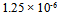
D:
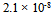
A:6.3/175
B:6.3/17.5
C:6.3/35
D:6.3/1.75
A:
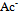
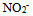
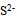
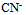
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!