第七章单元测试
- 写出
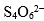 中S原子的氧化数( )。
中S原子的氧化数( )。 - 方程式
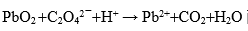 配平后的中,Pb的系数是( )。
配平后的中,Pb的系数是( )。 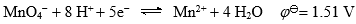 ,高锰酸钾是强氧化剂,因为它在反应中得的电子数多。( )
,高锰酸钾是强氧化剂,因为它在反应中得的电子数多。( )- 已知
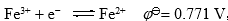 , 测定一个
, 测定一个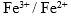 电极
电极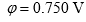 ,则溶液中必定是 ( )。
,则溶液中必定是 ( )。 - 下列氧化剂中增加
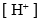 ,其氧化能力增强的物质是 ( )。
,其氧化能力增强的物质是 ( )。 - 两个半电池,电极相同,电解后溶液中各物质相同,都可以进行电极反应,但溶液浓度不同,将两个半电池用盐桥和导线联接,这个电池的电动势( )
- 用两铅片分别插入两
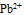 溶液中,做成电极I和II,分别得到电极电位:
溶液中,做成电极I和II,分别得到电极电位: 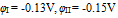 ,说明两溶液中
,说明两溶液中 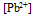 为( )
为( ) - 配平好下列反应:
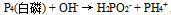 ,
,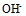 的系数是( )
的系数是( ) - 已知在酸性介质中,
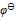
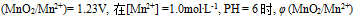 等于( )V
等于( )V - 将
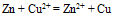 反应设计为原电池,若在铜半电池溶液中加入氨水后,则电池电动势E值将( )
反应设计为原电池,若在铜半电池溶液中加入氨水后,则电池电动势E值将( ) - 下列哪一个反应设计出来的电池不需要用到惰性电极材料( )
- 已知
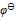
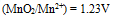 ,
, 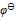
 , 从标准电极电势看,
, 从标准电极电势看, 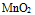 不能氧化
不能氧化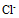 ,但用
,但用 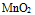 加浓盐酸,可以生成
加浓盐酸,可以生成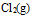 这是因为( )
这是因为( ) - 下列叙述中正确的是( )
- 电对
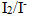 的
的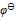 为0.534V,250C时,当
为0.534V,250C时,当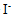 离子浓度为
离子浓度为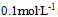 时的
时的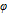 为( )
为( ) - 已知
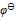
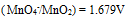 ,
, 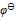
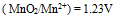 ,则
,则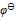
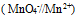 为( )
为( ) - 下列电对中,
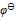 最大者是( )
最大者是( ) - 反应
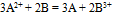 标准状态下电池电动势为1.80V,某浓度时,反应的电池电动势为1.60V,则此时该反应的lg
标准状态下电池电动势为1.80V,某浓度时,反应的电池电动势为1.60V,则此时该反应的lg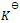 为( )
为( ) - 已知
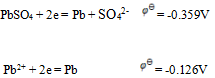
则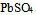 的溶度积为( )
的溶度积为( ) - 已知电极电势图:
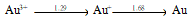
根据上列电势图可预测能自发进行的反应是( ) - 根据溴元素电势图:
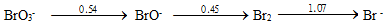
可求得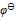 (BrO-/Br)为 ( )
(BrO-/Br)为 ( ) - 已知下列数据
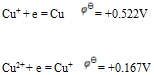
确定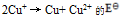 为( )
为( ) - 将反应Ni + Cu2+ = Ni2+ + Cu设计为原电池,下列哪一个为正确的电池符号? ( )
KMnO4与H2O2反应,可写出下列两个反应( )
(1)2KMnO4 +H2O2 +3H2SO4 = 2MnSO4 + K2SO4 +3O2+4H2O
(2)2KMnO4+5H2O2+3H2SO4 = 2MnSO4 + K2SO4 +5O2+4H2O
根据
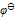 值判断下列各组离子在酸性介质中不能够共存的是( )
值判断下列各组离子在酸性介质中不能够共存的是( ) 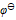 ( ClO3-/Cl-) =1.451V,
( ClO3-/Cl-) =1.451V, 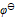 ( BrO3-/ Br2) =1.482V,
( BrO3-/ Br2) =1.482V, 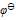 ( Fe3+/ Fe2+) = 0.771V,
( Fe3+/ Fe2+) = 0.771V,  ( Pb2+/ Pb) = - 0.126 V,
( Pb2+/ Pb) = - 0.126 V,  ( Sn4+/ Sn2+) =0.151V,
( Sn4+/ Sn2+) =0.151V,  ( I2/ I-) = 0.54V
( I2/ I-) = 0.54V有三个电池
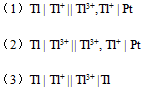
设这三个电池中各物质浓度都是
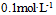 ,则它们的( )
,则它们的( )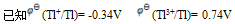
某溶液中含有
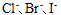 三种离子。要求只把
三种离子。要求只把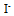 氧化出来而
氧化出来而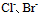 们留在溶液中,应选择哪种氧化剂( )。
们留在溶液中,应选择哪种氧化剂( )。已知:
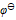
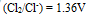 ,
,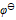
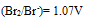 ,
,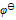
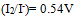
A:
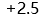
B:
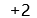
C:
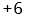
D:
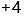
答案:
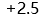
A:4
B:1
C:3
D:2
A:对 B:错
A:
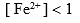
B:
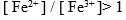
C:
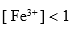
D:
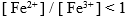
A:
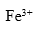
B:
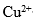
C:
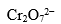
D:
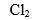
A:
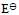 ≠0,
≠0, 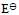 ≠ 0
≠ 0B:
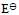 ≠0,
≠0, 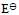 = 0
= 0C:
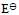 = 0,
= 0, 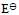 ≠ 0
≠ 0 D:
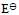 = 0,
= 0, 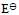 = 0
= 0 A:I > II
B:无法判断
C:II > I
D:I = II
A:3
B:1
C:2
D:4
A:1.94
B:0.52
C:0.71
D:1.23
A:增大
B:减小
C:无法判断
D:不变
A:
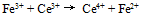
B:
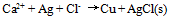
C:
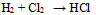
D:
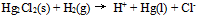
A:(两个
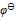 相差不太大 、酸度增加,
相差不太大 、酸度增加, 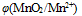 、
、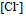 增加,
增加, 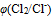 减小)三个因素都有
减小)三个因素都有 B:
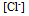 增加,
增加, 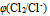 减小
减小 C:两个
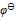 相差不太大
相差不太大 D:酸度增加,
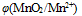
A:因为电对
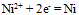 的
的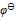 为-0.25v, 故
为-0.25v, 故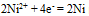 的
的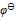 为-0.50v
为-0.50vB:因为
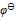
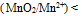
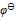
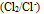 所以绝不能用
所以绝不能用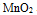 与盐酸作用制取
与盐酸作用制取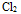
C:含氧酸根的氧化能力通常随溶液的pH值减少而增强
D:已知
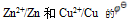 各为-0.762V和0.345V, 铜锌原电池的电动势之所以为1.105V, 原因在于
各为-0.762V和0.345V, 铜锌原电池的电动势之所以为1.105V, 原因在于 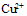 离子的浓度较
离子的浓度较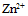 离子的大
离子的大A:0.650V
B:0.534V
C:0.593V
D:0.471V
A:0.635V
B:1.499V
C:1.825V
D:1.70V
A:
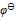
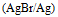
B:
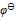
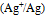
C:
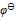
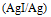
D:
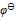
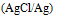
A:
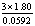
B:
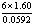
C:
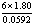
D:
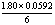
A:
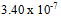
B:
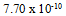
C:
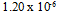
D:
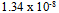
A:
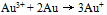
B:
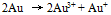
C:
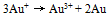
D:
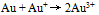
A:0.728V
B:1.52V
C:0.364V
D:0.76V
A:–0.689V
B:-0.355V
C:+0.689V
D:+0.355V
A:
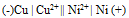
B:
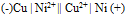
C:
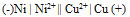
D:
A:(2)式对 B:(1)式对 C:两式都不对
A:Sn2+ 和I2 B:Fe2+ 和Pb2+ C:Fe2+ 和Sn4+ D:Br2和ClO3-
A:电池反应式相同,E相同 B:电池反应式不同,E相同 C:电池反应式不同,E不同 D:电池反应式相同,E不同
A:
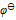
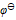
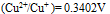
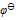
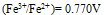
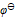
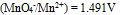
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!